企业档案
会员类型:会员

已获得易推广信誉 等级评定
(0 -40)基础信誉积累,可浏览访问
(41-90)良好信誉积累,可接洽商谈
(91+ )优质信誉积累,可持续信赖
易推广会员:8年
最后认证时间:
注册号: 【已认证】
法人代表: 【已认证】
企业类型:生产商 【已认证】
注册资金:人民币万 【已认证】
产品数:91228
参观次数:11306461
技术文章
Nrf2 的“戏精”之路
点击次数:626 发布时间:2021/8/3 13:16:30
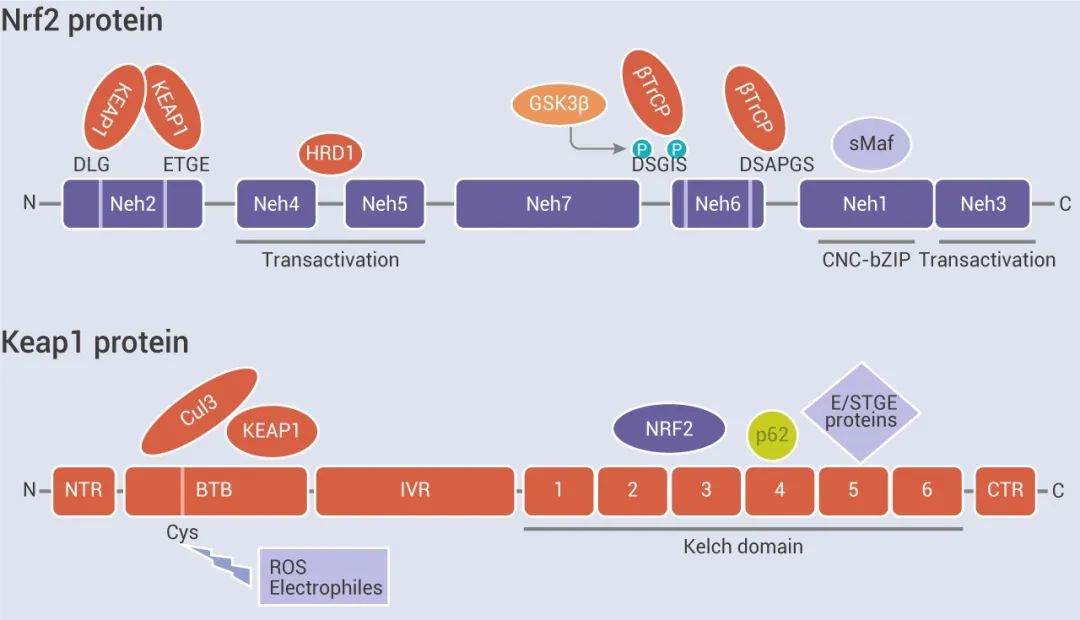
1、经典途径——Keap1-Nrf2 途径
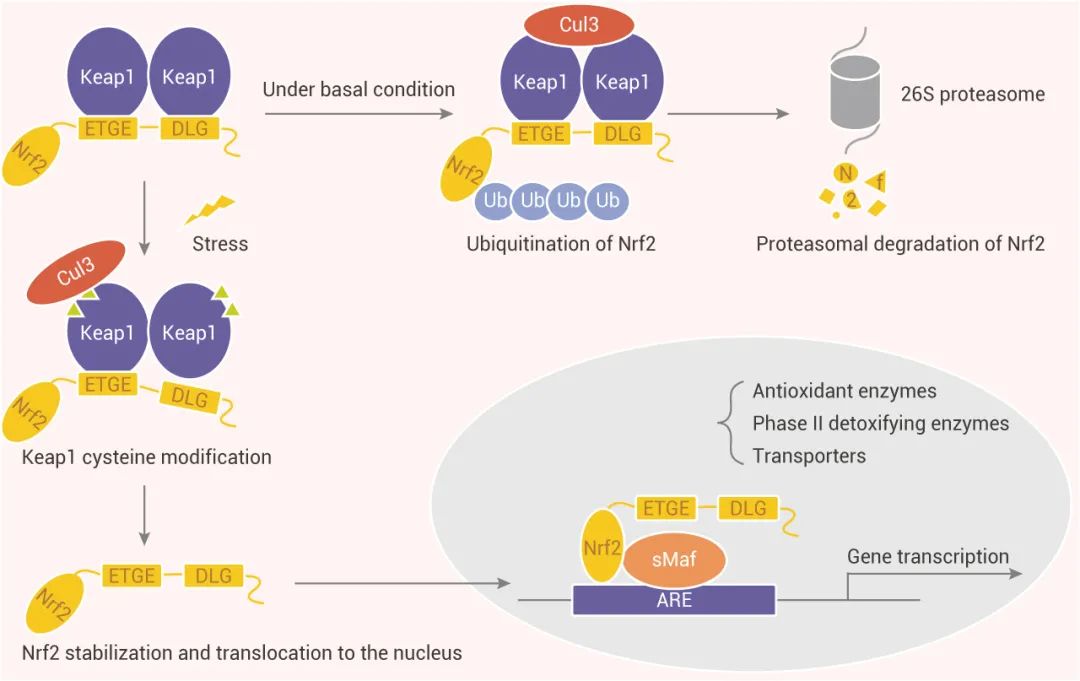
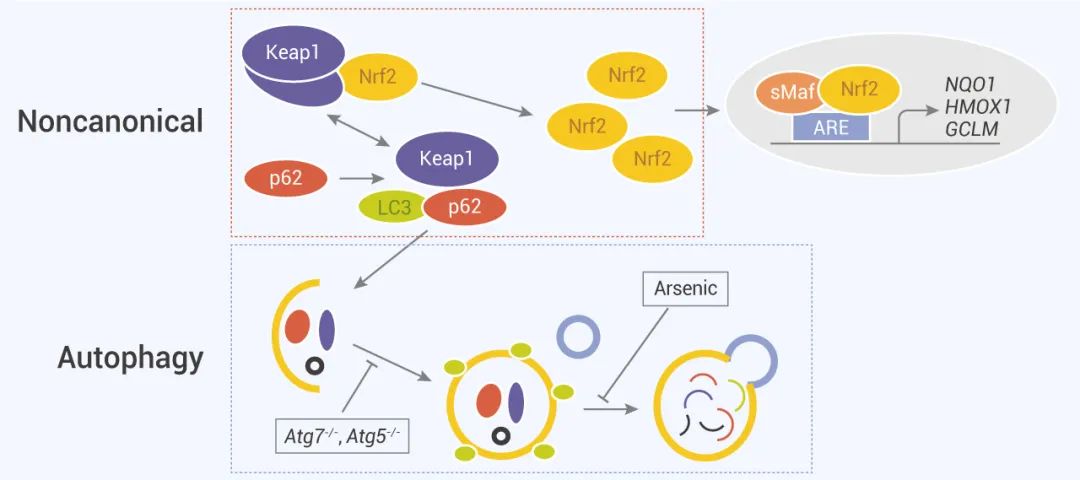
而暴露于 ROS、亲电胁迫会使 Keap1 中特定的半胱氨酸残基被修饰,引起 Keap1-Cul3-E3 泛素连接酶的构象变化,干扰 Nrf2 泛素化,随后 Nrf2 易位至细胞核,通过与 sMAF 蛋白的异二聚化作用结合到靶基因的 ARE/EpRE (抗氧化反应元件/亲电响应元件) ,诱导一系列细胞保护性基因表达,如 NQO1、GST、HMOX1、GCL、GSH 等。
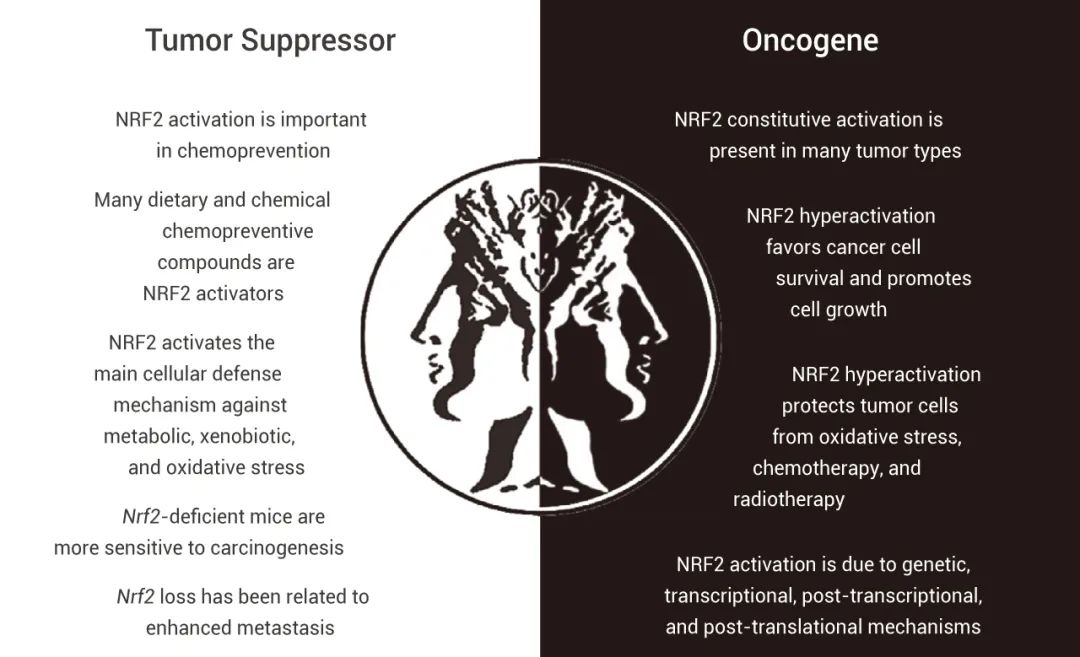
图 4. Nrf2 在癌症发生和发展中的双重作用[14]
Nrf2-Keap1 途径的激活是抗肿瘤发生的*重要机制。通过靶向 Nrf2/ARE 途径来调控基因,进而发挥化学预防作用的一些化合物,不仅包括合成化合物如 Oltipraz,还有一些植物来源的化合物,例如 Sulforaphane、Curcumin、Resveratrol 等。
一些研究表明在各种癌症中 Nrf2 信号通路组成性激活会促进癌细胞的生长和增殖,阻止细胞凋亡,增强癌症干细胞 (CSC) 的自我更新能力,更重要的是,可增强癌细胞的化学耐药性和放射抗性。因此,阻断 Nrf2 信号是一种有前途的癌症治疗方法,特别是对于 Nrf2 水平升高的癌症。靶向 Nrf2 的抑制剂也有很多,比如 Brusatol、ML385、Luteolin、Ochratoxin A、Retinoic acid (ATRA)、Trigonelline 等。
| Nrf2 激活剂 |
| 可以激活 Nrf2,并通过 AMPK 依赖性信号传导抑制高糖诱导的胰腺癌。 |
| 乙酰转移酶 p300/CREB 结合蛋白特异性抑制剂;通过 Keap1 半胱氨酸修饰诱导 Nrf2 蛋白的稳定。 |
| 广泛使用的 Nrf2 激活剂,通过激活 Nrf2 来免受 Doxorubicin (DOX) 诱导的心脏毒性。 |
| 天然多酚,具有抗氧化、抗炎、保护心脏和抗癌的特性。它的靶点广泛,例如 mTOR、JAK、β-amyloid、Adenylyl cyclase、IKKβ、DNA polymerase,也是 Nrf2 激活剂。 |
| 一种 HIF-1α 激活抑制剂,也是强效的 Nrf2 激活剂。 |
一种有效的核糖体 S6 激酶 (RSK2) 抑制剂;Nrf2 激活剂,能提高细胞核内 Nrf2 的水平。 |
| Nrf2 抑制剂 |
| 可抑制 Nrf2,通过一种不依赖于 Keap1、蛋白酶体和自噬蛋白降解系统的机制激发 Nrf2 的消耗。 |
| 有效的 Nrf2 抑制剂,具有抗炎和抗癌特性。 |
| RAR 核受体的天然激动剂,对 RARα/β/γ 作用的 IC50 为 14 nM;可以通过激活视黄酸受体抑制 Nrf2。 |
| 有潜在抗糖尿病活性的生物碱;有效的 Nrf2 抑制剂,能阻断 Nrf2 依赖性的蛋白酶体活性。 |
↓ 下滑查看更多文献
1. Tonelli C, et al. Transcriptional Regulation by Nrf2. Antioxid Redox Signal. 2018; 29(17): 1727-1745.
2. Rojo de la Vega M, et al. NRF2 and the Hallmarks of Cancer. Cancer Cell. 2018; 34(1): 21-43.
3. Qin JJ, et al. Dual roles and therapeutic potential of Keap1-Nrf2 pathway in pancreatic cancer: a systematic review. Cell Commun Signal. 2019; 17(1): 121.
4. Zhang DD, et al. Keap1 is a redox-regulated substrate adaptor protein for a Cul3-dependent ubiquitin ligase complex. Mol Cell Biol. 2004; 24(24): 10941-10953.
5. Canning P, et al. Structural basis of Keap1 interactions with Nrf2. Free Radic Biol Med. 2015; 88(Pt B): 101-107.
6. Jaramillo MC, et al. The emerging role of the Nrf2-Keap1 signaling pathway in cancer. Genes Dev. 2013; 27(20): 2179-2191.
7. Taguchi K, et al. Molecular mechanisms of the Keap1–Nrf2 pathway in stress response and cancer evolution. Genes Cells. 2011; 16(2): 123-140.
8. Zimta AA, et al. The Role of Nrf2 Activity in Cancer Development and Progression. Cancers (Basel). 2019; 11(11): 1755.
9. Wu S, et al. Nrf2 in cancers: A double-edged sword. Cancer Med. 2019; 8(5): 2252-2267.
10. Dodson M, et al. Non-canonical activation of NRF2: New insights and its relevance to disease. Curr Pathobiol Rep. 2017; 5(2): 171-176.
11. Silva-Islas CA, et al. Canonical and non-canonical mechanisms of Nrf2 activation. Pharmacol Res. 2018; 134: 92-99.
12. Katsuragi Y, et al. p62/SQSTM1 functions as a signaling hub and an autophagy adaptor. FEBS J. 2015; 282(24): 4672-4678.
13. Robledinos-Antón N, et al. Activators and Inhibitors of NRF2: A Review of Their Potential for Clinical Development. Oxid Med Cell Longev. 2019; 2019: 9372182.
14. Menegon S, et al. The Dual Roles of NRF2 in Cancer. Trends Mol Med. 2016; 22(7): 578-593.
15. Wu S, et al. Nrf2 in cancers: A double-edged sword. Cancer Med. 2019; 8(5): 2252-2267.
16. Jiang T, et al. p62 links autophagy and Nrf2 signaling. Free Radic Biol Med. 2015; 88(Pt B): 199-204.