企业档案
会员类型:会员

已获得易推广信誉 等级评定
(0 -40)基础信誉积累,可浏览访问
(41-90)良好信誉积累,可接洽商谈
(91+ )优质信誉积累,可持续信赖
易推广会员:8年
最后认证时间:
注册号: 【已认证】
法人代表: 【已认证】
企业类型:生产商 【已认证】
注册资金:人民币万 【已认证】
产品数:91228
参观次数:11304740
技术文章
MCE | 铁死亡――调节性细胞死亡
点击次数:595 发布时间:2021/8/28 15:55:29
“铁死亡”这一概念*早在 2012 年由 Dr. Brent R Stockwell 提出,它是一种铁离子依赖的新型细胞调节性死亡,在细胞形态学上,生化特征区别于细胞凋亡、坏死、自噬。从机制上简单来说,铁死亡是细胞膜上铁依赖性的高表达的不饱和脂肪酸,发生脂质过氧化,诱导的细胞死亡。
近年来,铁死亡相关研究是如火如荼,前途一片光明。今年 1 月,广州医科大学唐道林教授团队在 Nat Rev Clin Oncol 上发表题为 Broadening horizons: the role of ferroptosis in cancer 的综述。
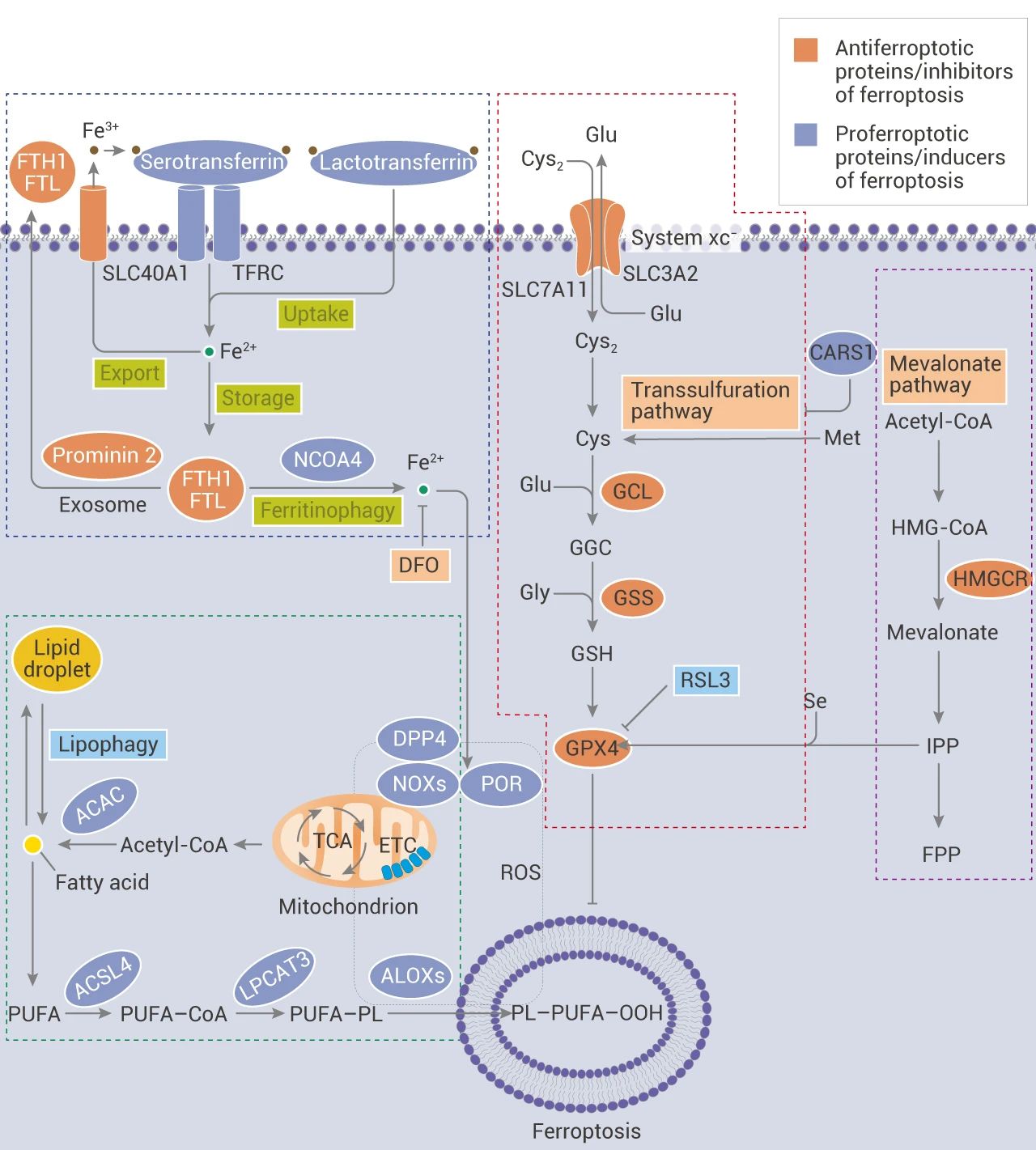
图 1. 铁死亡在癌症中的作用[1]
在这篇高分综述中,关于铁死亡,作者提出了几个观点:
1、铁死亡 (Ferroptosis) 是一种调节性的细胞死亡,依赖于铁介导的氧化损伤。
■ 外源性 (转运蛋白依赖) 途径
1、抑制胱氨酸/谷氨酸反向转运蛋白来促进铁死亡
System xc- 是细胞内重要的抗氧化体系,该系统由 2 个亚基组成,SLC7A11 和 SLC3A2。SLC7A11 负责主要的转运活性,对胱氨酸和谷氨酸有高度特异性,而 SLC3A2 则作为伴侣蛋白。System xc- 以 1:1 的比例用胞内谷氨酸来换取胞外的胱氨酸 (Cys2),胱氨酸在谷氨酸半胱氨酸连接酶 (GCL) 和谷胱甘肽合成酶 (GSS) 的催化作用下合成谷胱甘肽 (GSH)。
GSH 是膜脂修复酶——谷胱甘肽过氧化物酶 (GPX4) 的还原性辅因子。抑制 System xc- 的活性会抑制胱氨酸的吸收,影响 GSH 的合成,继而导致膜脂修复酶 GPX4 活性降低,细胞抗氧化能力降低,从而促进铁死亡。
增加铁的吸收,减少铁的储存和限制铁的外流都会导致铁积累增加,然后通过一系列的信号传导途径来促进铁死亡。
转铁蛋白 (血清转铁蛋白或乳铁蛋白) 通过转铁蛋白受体 (TFRC) 介导铁摄取,FTH1/FTL (铁蛋白组件) 通过自噬降解可以增加铁的水平,这些都可以促进铁死亡。而 SLC40A1 介导的铁外流和外泌体介导的铁蛋白输出会抑制铁死亡。
■ 内源性 (酶调控) 途径
内源性途径是通过阻断细胞内抗氧化酶 (如 GPX4) 激活的。
1、抑制 GPX4 诱导铁死亡
脂质过氧化物积累是铁死亡的标志。GPX4 可将细胞毒性脂质过氧化物 (L-OOH) 还原为相应的醇 (L-OH),抑制 GPX4 活性会导致细胞膜脂质过氧化物的积累。
直接抑制:如 RSL3 作为铁死亡诱导剂,可直接作用于 GPX4 并抑制其活性,因此降低了细胞的抗氧化能力并积累了 ROS,从而导致铁死亡。
2、其他酶的调节途径与脂肪酸积累
乙酰辅酶 A 羧化酶 (ACAC) 介导的脂肪酸合成,脂质吞噬 (Lipophagy) 介导的脂肪酸释放,可诱导细胞内游离脂肪酸的积累,促进铁死亡。
长链脂肪酸辅酶 A 连接酶 4 (ACSL4) 和溶血磷脂酰基转移酶 3 (LPCAT3) 促进多不饱和脂肪酸 (PUFA) 掺入磷脂中形成多不饱和脂肪酸的磷脂 (PUFA-PL)。PUFA-PLs 易受脂氧合酶 (ALOXs) 介导的自由基引发的氧化作用。这种氧化作用*终会导致脂质双层的破坏并影响膜功能,从而促进铁死亡。
上文介绍了铁死亡的基本途径。铁死亡有哪些研究策略呢?下面以文献 Energy-stress-mediated AMPK activation inhibits ferroptosis 为例。
作者团队建立了特定病理过程 (铁死亡) 的细胞模型,使用多种诱导剂和抑制剂,以及多种检测方法证明铁死亡与 AMPK 的调控关系,并建立了 AMPKα1/α2 的基因敲除细胞系 (AMPK DKO),验证 AMPK 缺失对铁死亡敏感性的作用机制。
■ 确立铁死亡病理模型
1、能量应激 (Energy stress) 抑制铁死亡
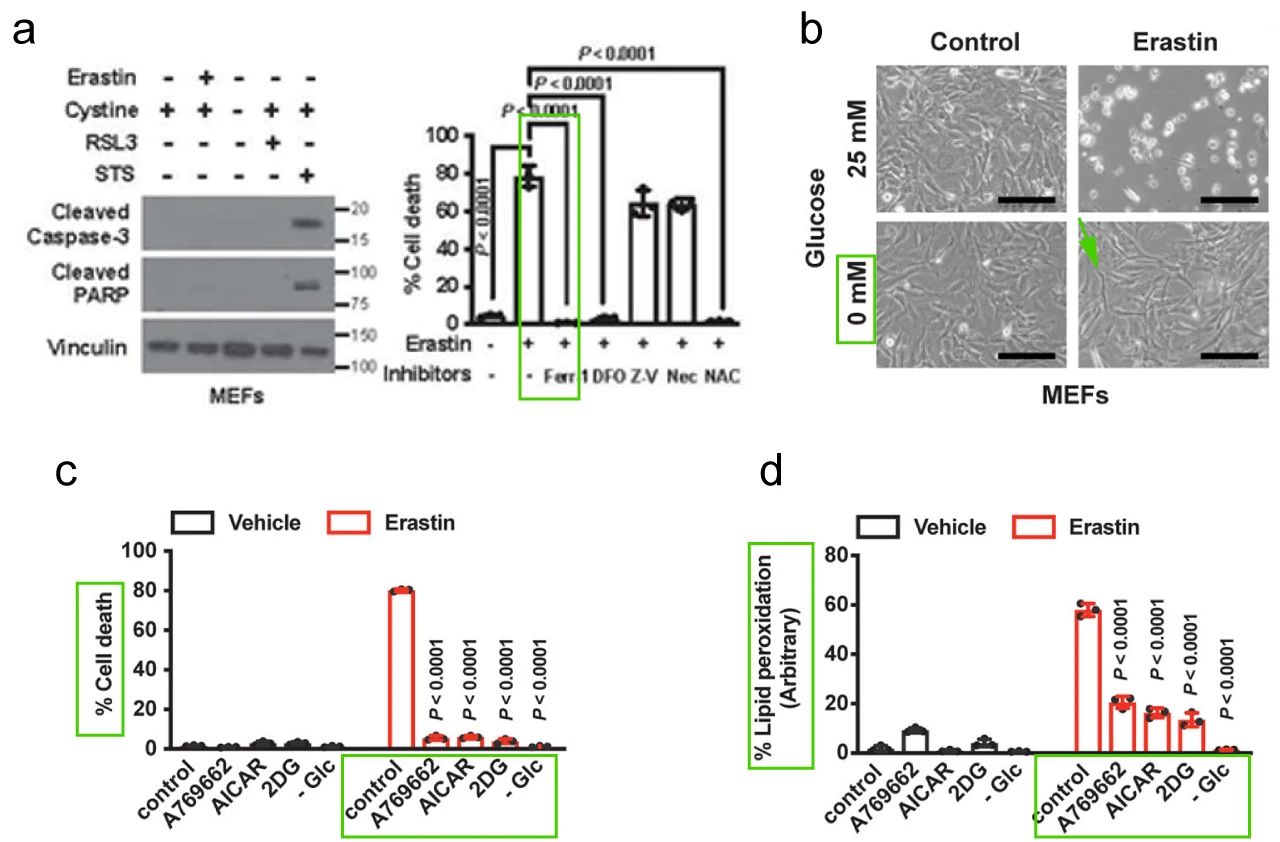
首先,研究人员探索了永生化小鼠胚胎成纤维细胞 (MEFs) 中,葡萄糖饥饿条件对 Erastin 诱导的铁死亡的影响。首先,证明 Erastin 诱导铁死亡:Caspase-3 或 PARP 裂解均未下调 (细胞凋亡的标志),而且铁死亡抑制剂 Ferrostatin-1 可以逆转 Erastin 诱导的细胞死亡。*初他们预想,葡萄糖饥饿的条件会增强 Erastin 诱导的铁死亡,结果恰恰相反:葡萄糖饥饿很大程度上逆转了 MEFs 中引起的铁死亡。
作者团队进一步选择了其他可诱导或模拟能量应激的化合物,包括 2-脱氧葡萄糖 (2-DG)、阿卡地新 (AICAR)、A769662。这些化合物也显著抑制了由 Erastin 处理引起的脂质过氧化和铁死亡。综上所述,能量应激抑制了铁死亡。
2、AMPKα1/α2 的基因敲除细胞系建立
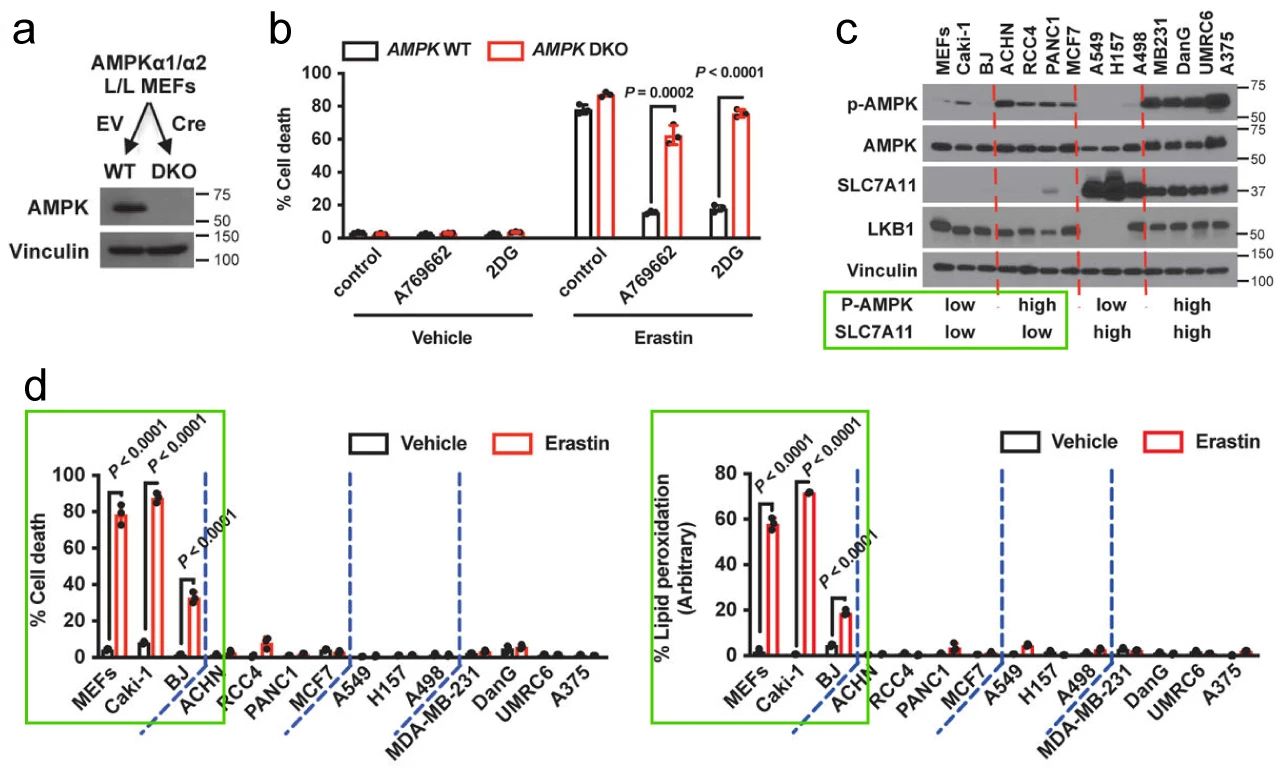
上述模拟或诱导能量应激的化合物均会激活 AMPK,那么 AMPK 是否参与能量应激介导的铁死亡抑制?MEFs 中,如图 4a-b,AMPK 双敲除 (DKO) 可以逆转诱导能量应激的化合物对 Erastin 诱导的铁死亡的抑制作用。
紧接着,如图 4c,作者又验证了一组细胞系中的基础 AMPK 激活状态 (p-AMPK Thr172 为激活标志) 与铁死亡 (SLC7A11 的表达水平) 相关性。并且如图 4c-d 所示,SLC7A11 高表达细胞相对于低表达细胞对铁死亡的抵抗力更高,值得注意的是,虽然在 SLC7A11 高表达细胞中 AMPK 激活状态与铁死亡的敏感性无关,但 SLC7A11 低表达细胞中 AMPK 的激活与铁死亡敏感性呈负相关。以上数据表明能量应激部分通过 AMPK 抑制了铁死亡。
3、AMPK 失活使癌细胞对铁死亡敏感
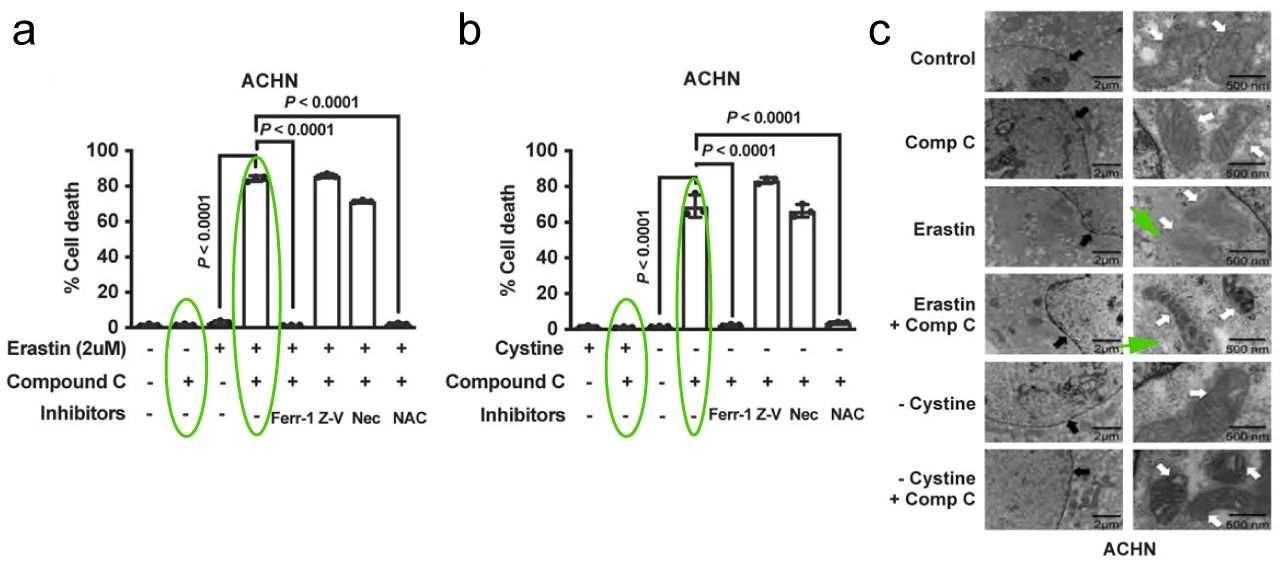
AMPK 在高基础 AMPK 磷酸化水平的癌细胞系中是否会促进铁死亡抗性?AMPK 抑制剂 Compound C 可下调 AMPK 的激活,如图 5a-b,Compound C 处理使 ACHN 细胞 (高基础 AMPK 磷酸化的抗铁碱化细胞系) 对 Erastin 或胱氨酸耗竭变敏感。透射电子显微镜 (TEM) 的结果也显示,ACHN 细胞中,Compound C 与 Erastin 或胱氨酸耗竭共同处理导致线粒体收缩,膜密度增加,但细胞核中没有明显的 DNA 片段化 (铁死亡的细胞特征形态特征)。这表明 AMPK 的抑制使癌细胞对铁死亡敏感。
图 5. Erastin 或胱氨酸耗竭条件下 ACHN 细胞对铁死亡的敏感性
(a-b. CCK8 法和脂质过氧化测定法检测,Erastin 或胱氨酸耗竭条件下 ACHN 细胞对铁死亡的敏感性;c. 透射电子显微镜 (TEM) 分析)
总结:
1、GSH-GPX4 抗氧化系统在铁死亡途径中起重要作用。脂质过氧化物增加,转铁蛋白等介导的铁的积累,以及细胞内游离脂肪酸的积累都可以诱导铁死亡。
2、Hyemin Lee 等人使用铁死亡通路相关的抑制剂/诱导剂,以及建立了 AMPK 敲除细胞系,证明铁死亡与 AMPK 之间的调节关系。
3、常见的检测铁死亡的实验方法:铁死亡相关细胞存活分析,如文中的 CCK8 法 (其他细胞活力检测方法还包括 MTT 法,台盼蓝染色等)。
4、除了细胞活力测定,脂质氧化水平的测定 (文中的 C11 BODIPY 581/591 染色),GSH 测定,线粒体 ROS 测定,以及 GPX4 活性测定,电镜下线粒体的变化的监测,特异性靶标分子的分析 (WB、IHC、IF 等) 也是常用的检测手段。
| 相关产品 |
| 铁死亡诱导剂,结合且抑制电压依赖性阴离子通道 (VDAC2/VDAC3)。 |
| 铁死亡诱导剂,可直接降低 GPX4 的表达。 |
| 一种氨基酸,在细胞调节过程中起着重要作用,胱氨酸耗竭会诱导铁死亡。 |
| 选择性的铁死亡抑制剂,人工合成的抗氧化剂,通过还原机制来防止膜脂的损伤,从而抑制细胞死亡。 |
| 腺苷类似物,也是一种 AMPK 激活剂,调节葡萄糖和脂质的代谢。 |
| 有效的,可逆的 AMPK 激活剂,EC50 值为 0.8 μM。 |
| 选择性 AMPK 抑制剂,可参与细胞自噬以及铁死亡。 |
细胞活性和细胞毒性检测的快速、高灵敏度试剂盒。 |
| 可用于细胞增殖,活性毒性的检测。 |
| 可渗透细胞的,用于检测细胞内活性氧 (ROS) 水平的探针。 |
| 用于测量线粒体膜电位的荧光探针试剂盒。 |
| 亲脂性红色荧光染料,可用于线粒体膜电位检测。 |
| 收集了 500+ 种文献报道的具有诱导或抑制铁死亡相关的化合物及与铁死亡密切相关的靶点对应的化合物,可以用于铁死亡机制及相关疾病的研究。 |
MCE 的所有产品仅用作科学研究或药证申报,我们不为任何个人用途提供产品和服务
RCD: Regulated cell death
↓ 下滑查看更多文献
1. Daolin Tang, Xin Chen, Rui Kang, Guido Kroemer. Broadening horizons: the role of ferroptosis in cancer. Nat Rev Clin Oncol. 2021 Jan 29.
2. Hyemin Lee, et al. Energy-stress-mediated AMPK activation inhibits ferroptosis. Nat Cell Biol. 2020 Feb; 22(2): 225-234.