企业档案
会员类型:会员

已获得易推广信誉 等级评定
(0 -40)基础信誉积累,可浏览访问
(41-90)良好信誉积累,可接洽商谈
(91+ )优质信誉积累,可持续信赖
易推广会员:8年
最后认证时间:
注册号: 【已认证】
法人代表: 【已认证】
企业类型:生产商 【已认证】
注册资金:人民币万 【已认证】
产品数:91228
参观次数:11305264
技术文章
MCE | 肿瘤微环境在癌症中的作用
点击次数:535 发布时间:2021/8/31 10:46:05
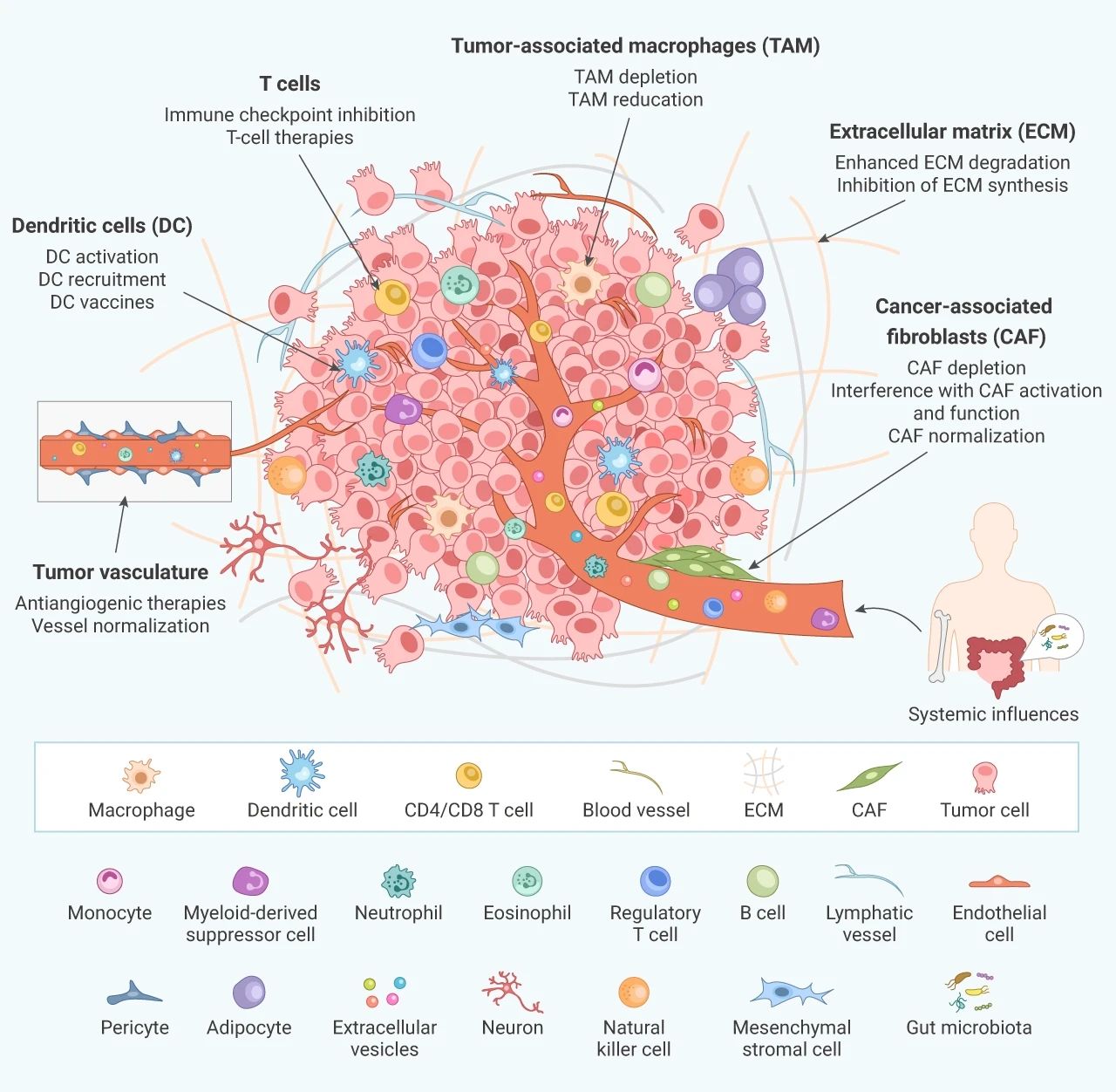
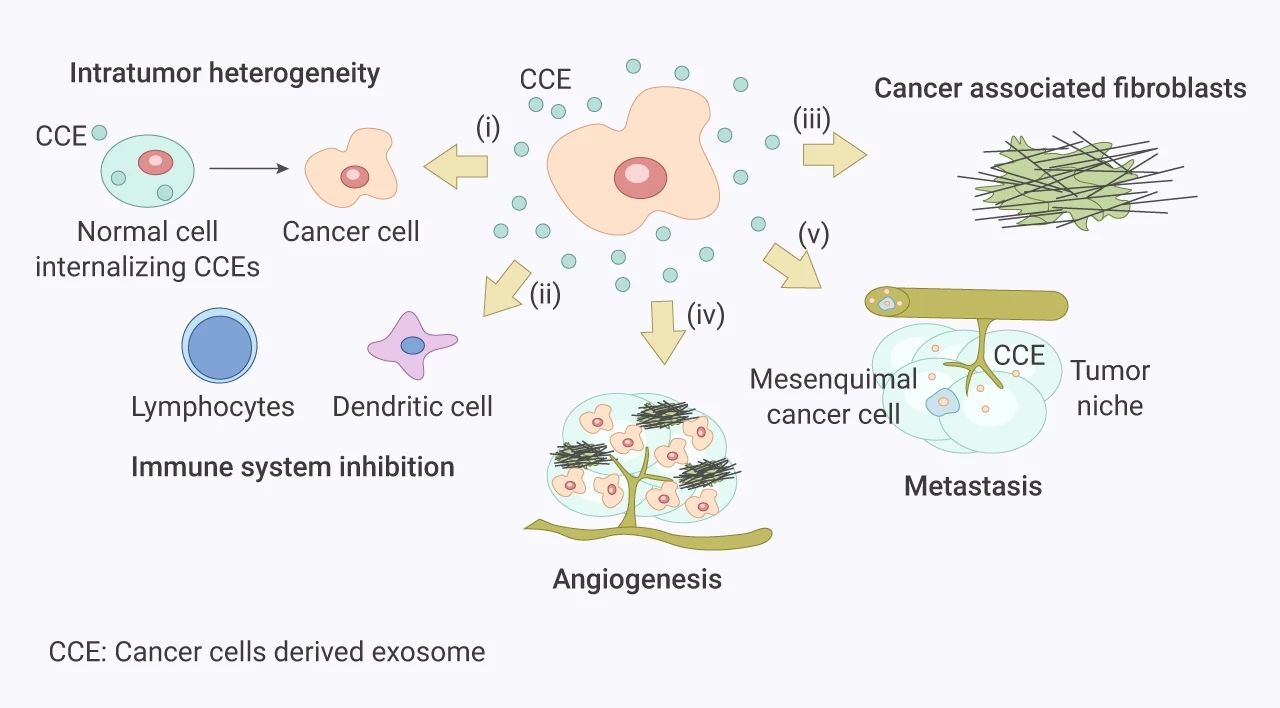
肿瘤细胞和微环境之间的通讯机制很复杂,主体分为:1) 特定癌细胞与另一个细胞或细胞与 ECM 之间的依赖接触性机制;2) 可溶性分子 (生长因子、趋化因子、细胞因子以及亚细胞结构,包括微囊泡和外泌体) 的非依赖接触机制。这些相互作用通过近分泌和旁分泌机制、恶性细胞和非恶性基质细胞中的信号通路激活,在癌症的进展过程中发挥重要作用,如诱导增殖和抑制细胞凋亡、诱导血管生成和避免缺氧、抑制免疫系统以及远处转移等。因此,靶向肿瘤微环境是一种预防转移、克服获得性耐药和提高治疗效果的具有广阔前景的策略。
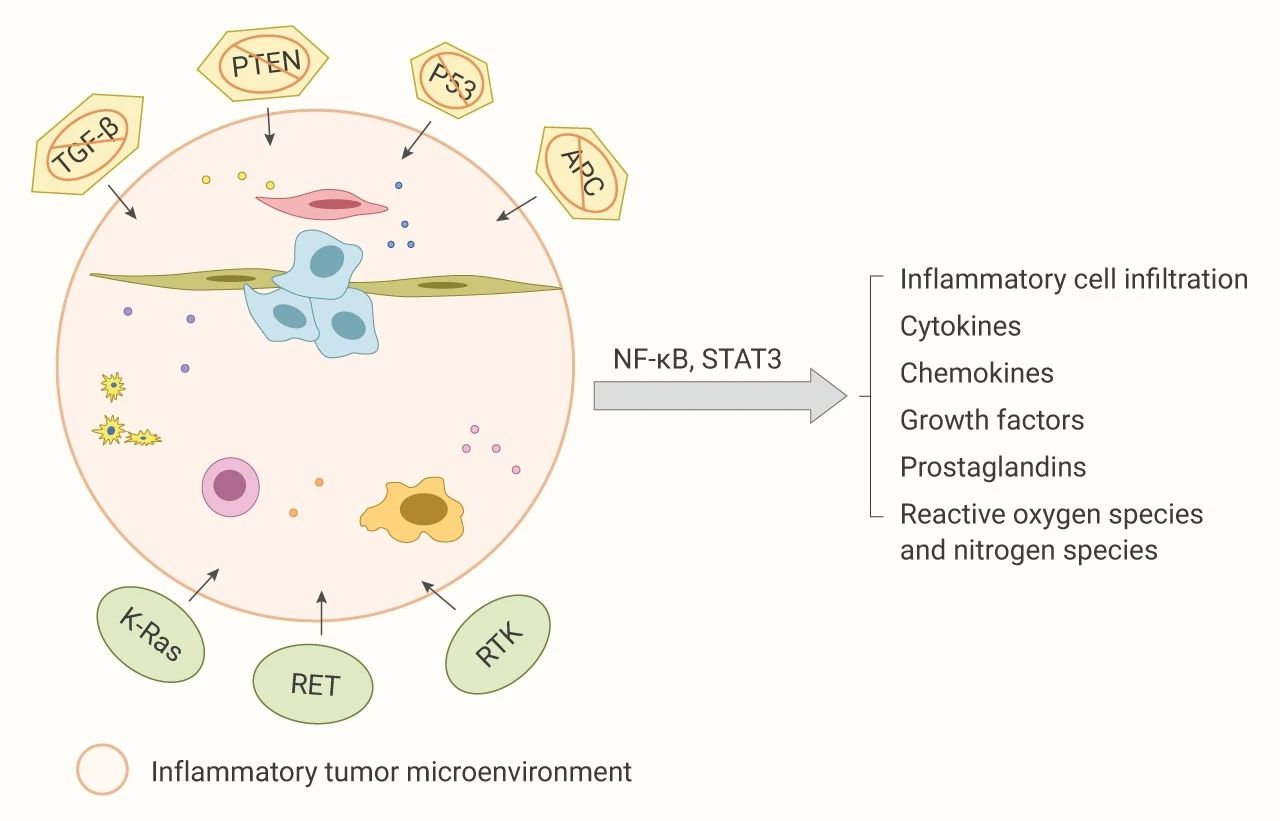
图 2. 肿瘤抑制因子丢失或致癌基因的激活诱导的炎症微环境
■ 激活免疫系统的抗肿瘤活性
| 相关产品 |
| 高选择性,有口服活性的 VEGFR2 抑制剂,对 Flt1, KDR, Flt4, PDGFRα, PDGFRβ, c-Kit 的 IC50 值分别为 <1 nM, <3 nM, 5 nM, 5 nM, 36 nM, 2 nM。 |
| ATP 竞争性的 VEGFR2 抑制剂,IC50 值为 25 nM。可以适度抑制 VEGFR1 和 FGFR1。 |
| 特异性的 mTOR 抑制剂,作用于 HEK293 细胞,抑制 mTOR,IC50 为 0.1 nM。Rapamycin 与 FKBP12 结合且抑制 mTORC1。Rapamycin 还是一种自噬 (autophagy) 激活剂,免疫抑制剂。 |
| 一种有效,选择性和可透过血脑屏障的 CSF-1R (c-Fms) 抑制剂,IC50 为 1 nM,选择性是其他受体酪氨酸激酶同系物的 1000 倍。 |
| 通过对不同途径调控,如 NF-κB、Akt、IL-6/JAK2/STAT3 及其下游靶蛋白,显著抑制肿瘤的增殖、存活、血管生成、侵袭和转移,显示出其抗癌作用。 |
| 特异性 STAT3 抑制剂,抑制 G-CSF 诱导的 STAT3 磷酸化,诱导 AML 细胞系和原代标本的凋亡,并在低微摩尔范围内抑制 AML 细胞集落形成。 |
| 选择性的 COX-2 抑制剂,IC50 为 40 nM。 |
| 选择性的 CXCR4 拮抗剂,IC50 为 44 nM。防止 肿瘤相关巨噬细胞 (TAM) 浸润到肿瘤组织中。 |
| 选择性的 CCR5 拮抗剂,具有抑制 HIV 的活性。显著降低肿瘤相关巨噬细胞 (TAM) 浸润和肿瘤生长。 |
| HSP90 抑制剂,通过抑制 HIF-1α 和 STAT3 对结直肠癌具有抗血管生成作用。 |
MCE 的所有产品仅用作科学研究或药证申报,我们不为任何个人用途提供产品和服务
参考文献
下滑查看更多 ↓
1. Global Burden of Disease Cancer Collaboration, Fitzmaurice C, et al. Global, Regional, and National Cancer Incidence, Mortality, Years of Life Lost, Years Lived With Disability, and Disability-Adjusted Life-Years for 29 Cancer Groups, 1990 to 2016: A Systematic Analysis for the Global Burden of Disease Study. JAMA Oncol. 2018;4(11):1553-1568.
2. Pitt JM, Zitvogel L, et al. Targeting the tumor microenvironment: removing obstruction to anticancer immune responses and immunotherapy. Ann Oncol. 2016;27(8):1482-1492.
3. Martin M, et al. Targeting microenvironment in cancer therapeutics. Oncotarget. 2016;7(32):52575-52583.
4. Wu J, et al. Tumor microenvironment as the "regulator" and "target" for gene therapy. J Gene Med. 2019;21(7):e3088.
5. Chen F, Sun Y, et al. New horizons in tumor microenvironment biology: challenges and opportunities. BMC Med. 2015;13:45. Published 2015 Mar 5.
6. Wu T, Dai Y. Tumor microenvironment and therapeutic response. Cancer Lett. 2017;387:61-68.
7. Butturini E, Mariotto S. Tumor Dormancy and Interplay with Hypoxic Tumor Microenvironment. Int J Mol Sci. 2019;20(17):4305. Published 2019 Sep 3.
8. Casey SC, Felsher DW, et al. Cancer prevention and therapy through the modulation of the tumor microenvironment. Semin Cancer Biol. 2015;35 Suppl(Suppl):S199-S223.
9. Bejarano L, Jordāo MJC, Joyce JA. Therapeutic Targeting of the Tumor Microenvironment. Cancer Discov. 2021;11(4):933-959.
10. Roma-Rodrigues C, Baptista PV, Fernandes AR, et al. Targeting Tumor Microenvironment for Cancer Therapy. Int J Mol Sci. 2019;20(4):840. Published 2019 Feb 15.
11. Conciatori F, Ciuffreda L et al. Role of mTOR Signaling in Tumor Microenvironment: An Overview. Int J Mol Sci. 2018;19(8):2453. Published 2018 Aug 19.
12. Zhou K, et al. Targeting tumor-associated macrophages in the tumor microenvironment. Oncol Lett. 2020;20(5):234.
13. Achyut BR, Arbab AS. Myeloid cell signatures in tumor microenvironment predicts therapeutic response in cancer. Onco Targets Ther. 2016;9:1047-1055. Published 2016 Mar 1.
14. Hsieh CH, et al. Snail-overexpressing Cancer Cells Promote M2-Like Polarization of Tumor-Associated Macrophages by Delivering MiR-21-Abundant Exosomes. Neoplasia. 2018;20(8):775-788.
15. Fang H, Declerck YA. Targeting the tumor microenvironment: from understanding pathways to effective clinical trials. Cancer Res. 2013;73(16):4965-4977. 1
16. Yang L, Lin PC. Mechanisms that drive inflammatory tumor microenvironment, tumor heterogeneity, and metastatic progression. Semin Cancer Biol. 2017;47:185-195.
17. Roma-Rodrigues C, et al. Exosome in tumour microenvironment: overview of the crosstalk between normal and cancer cells. Biomed Res Int. 2014;2014:179486.
18. Anari F, Zibelman M, et al. Impact of tumor microenvironment composition on therapeutic responses and clinical outcomes in cancer. Future Oncol. 2018;14(14):1409-1421.