动物心脏电生理导管,动物心脏电生理研究系统
企业档案
会员类型:会员

已获得易推广信誉 等级评定
(0 -40)基础信誉积累,可浏览访问
(41-90)良好信誉积累,可接洽商谈
(91+ )优质信誉积累,可持续信赖
易推广会员:5年
最后认证时间:
注册号:**** 【已认证】
法人代表: 【已认证】
企业类型:个体商户 【已认证】
注册资金:人民币***万 【已认证】
产品数:1550
参观次数:839726
详细内容
动物心功能研究系统用于较为全面评估动物心脏功能,包括心脏收缩舒张功能、泵血功能、血流动力学、心脏电生理学等,其由动物压力测量系统、心室压力-容积测量系统及心脏电生理测量系统组成,3 系统各自独立,且均由 Scisence 固态导管系统及 iWorx 数据采集系统组成。
电生理导管系统
传统动物心电图测量分析采用体表无创方式,虽操作简单,但是存在测量位置影响大、测量精度不高等局限性,而心外膜表面电测量心电图操作为复杂且创伤性大,实验中较少采用。为解决这一难题,Scisence 提供微创的多电电生理导管,独特设计使研究者能够对生物电在整个心脏的扩散过程进行更为深入的测量和分析。

电生理导管系统由八电电生理导管、电分配盒及第三方生物电放大器及刺激器组成。
工作原理:八电电生理导管上的每对电均独立受控于电分配盒,电分配盒通过 2mm 针式连接线与第三方生物电放大器或刺激器相连,通过生理记录仪采集对应的电对引导的电信号数据。八电电生理导管可用于心脏起搏,电信号记录,进而用于心脏电生理的各方面研究。

电生理导管可插入大小鼠等动物的心脏内部,纪录心房及心室的电生理信号:传导时间、不应期、希氏束电位、窦房结和房室结功能、心律失常的诱导。
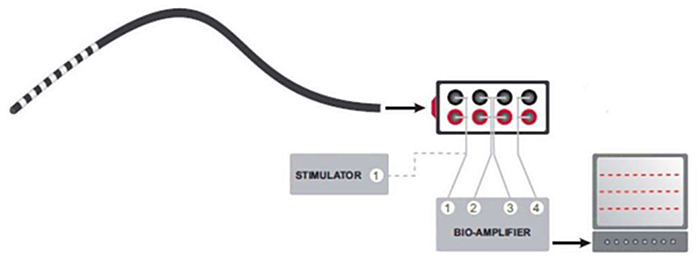
电生理导管系统特点
1. 微创八电电生理导管,可监测心内各个部位的心电信号
2. 多可同时引导心内 4 个不同部位的心电信号,可观察心电信号的扩散过程
3. 同一根导管可同时用于采集信号和给予刺激
4. 小鼠 1.1F,电间距 0.5mm;大鼠 1.9F,电间距 1.0mm;导管电间距可定制
5. 聚酰胺材料制作,生物相容性好,兼顾灵活性和刚性,光滑而便于插入
6. 电分配盒独立控制每对电,电之间互不影响
7. 兼容多种第三方生物电放大器、刺激器、数据采集器,如美国 iWorx 的 iWire-BIOx、IX-RA-834 等
8. 动物实验用,不能用于人体
LabScribe 心电分析模块
1. 测量心电图 R-R、PR、QT、TP、QR、QTc 间隔,QRS、T、P 波宽,P、Q、R、S、T 波幅以及 ST段抬高等数据;2. 具有具体的分析模板,可准确描绘各波起点、波宽、波幅等;
3. 客户可定制门的 ECG 模板,以满足自身特殊实验的需要;
4. 可从 R-R 间期、心率、噪音和活动性等方面来划定异常值,从而使分析更准确。
5. 可轻松提取源数据或平均数据作为图片或文本导出;
6. 可选 ASCII 文本导入模块将其他第三方设备采集的 ECG 数据导入本软件进行分析;
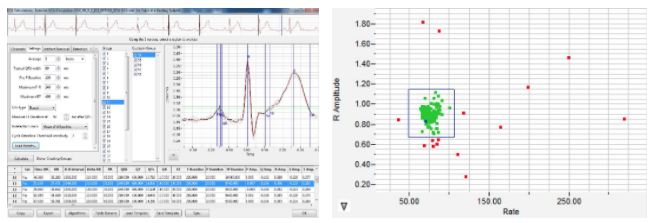
LabScribe 心电分析
相关文献
Luo X, et. al. “MicroRNA-26 governs profibrillatory inward-rectifier potassium current changes in atrial fibrillation.” J Clin Invest. 2013 May 1; 123(5): 1939-51
De Jong AM, et. al. “Atrial remodeling is directly related to end-diastolic left ventricular pressure in a mouse model of ventricular pressure overload.” PLoS One. 2013 Sep 6; 8(9): e72651
Guasch E, et. al. “Atrial fibrillation promotion by endurance exercise: demonstration and mechanistic exploration in an animal model.” J Am Coll Cardiol. 2013 Jul 2;62(1):68-77
Cardin S, et. al. “Role for MicroRNA-21 in atrial profibrillatory fibrotic remodeling associated with experimental postinfarction heart failure.” Circ Arrhythm Electrophysiol. 2012 Oct; 5(5): 1027-35
Iwasaki YK, et. al. “Determinants of atrial fibrillation in an animal model of obesity and acute obstructive sleep apnea.” Heart Rhythm. 2012 Sep; 9(9): 1409-16.e1
Jiao KL, et. al. “Effects of valsartan on ventricular arrhythmia induced by programmed electrical stimulation in rats with myocardial infarction.” J Cell Mol Med. 2012 Jun; 16(6): 1342-51
Zhou Y, et. al. “Matrine inhibits pacing induced atrial fibrillation by modulating I(KM3) and I(Ca-L).” Int J Biol Sci. 2012; 8(1): 150-8.
Benito B, et. al. “Cardiac arrhythmogenic remodeling in a rat model of long-term intensive exercise training.” Circulation. 2011 Jan 4; 123(1): 13-22
Prestia KA, et al. “Increased Cell-Cell Coupling Increases Infarct Size and Does not Decrease Incidence of Ventricular Tachycardia in Mice.” Front Physiol. 2011 Jan 31; 2(1): 1-7
Aubin MC, et al. “A high-fat diet increases risk of ventricular arrhythmia in female rats: enhanced arrhythmic risk in the absence of obesity or hyperlipidemia.” J Appl Physiol. 2010 Feb; 108: 933-940
Lu Y, et al. “MicroRNA-328 contributes to adverse electrical remodeling in atrial fibrillation.” Circulation. 2010 Dec; 122(23): 2378-87
Mathur N, et al. “Sudden infant death syndrome in mice with an inherited mutation in RyR2.” Circ Arrhythm Electrophysiol. 2009 Dec; 2: 677-685
您想了解更多详细资料吗?
请与我们联系:
TEL : 021-35183767 , 18502129044
QQ : 3007536034
Mail: yuyan0317@126.com
敬请来电咨询!










